重要發現與突破
植微所(5)
細生所(4)
生化所(3)
生醫所(5)
分生所(3)
多樣中心(18)
陳可萱 CHEN, KO-HSUAN
Science Advances
12 Feb 2025
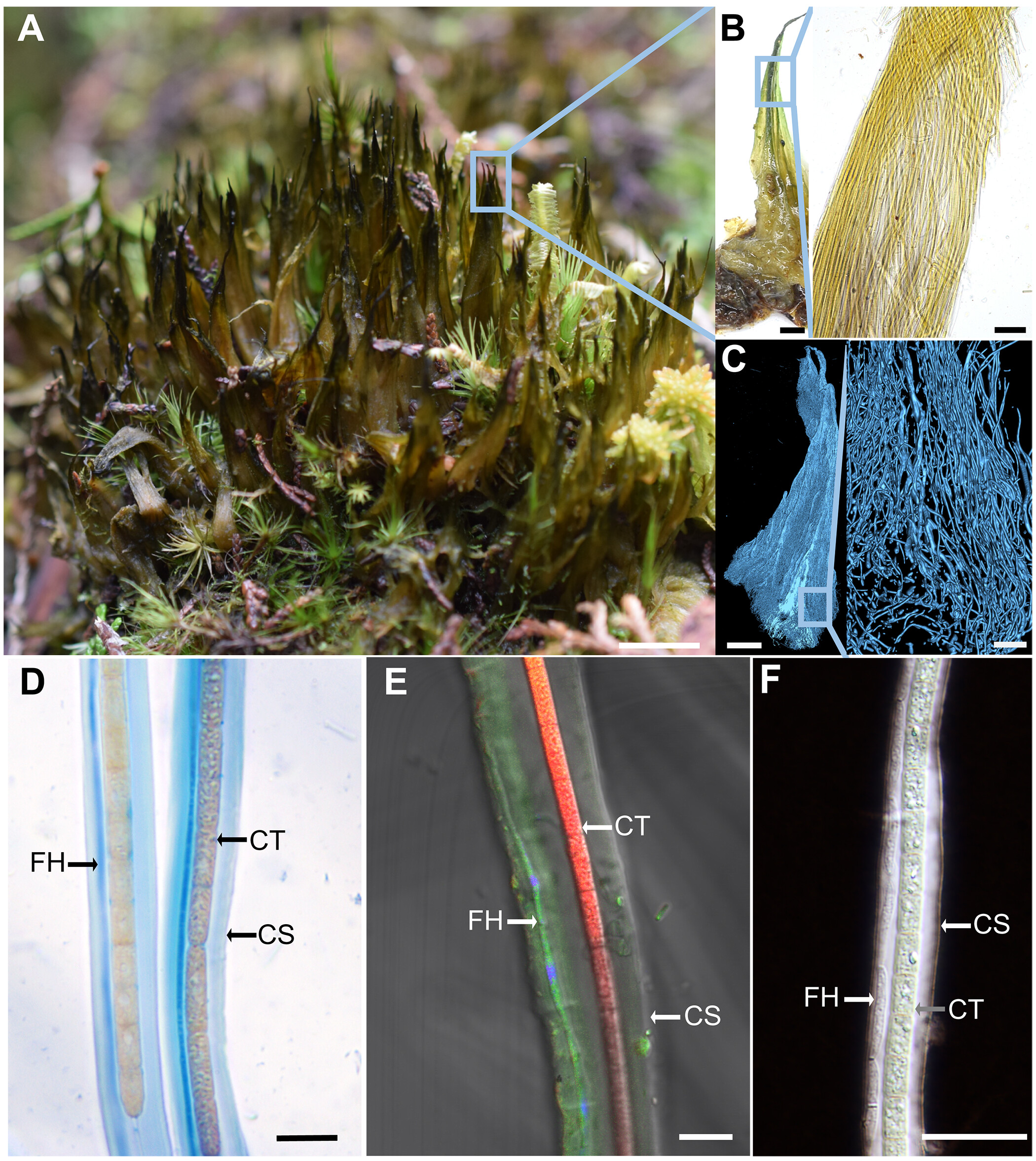
A thallus forming N-fixing fungus-cyanobacterium symbiosis from subtropical forests

Science Advances
12 Feb 2025
A thallus forming N-fixing fungus-cyanobacterium symbiosis from subtropical forests