本文由訊聯基因數位股份有限公司(原名:創源生技)提供
Qiagen Ingenuity pathway analysis (IPA) 是生物科學領域中路經分析的先驅,IPA 提供了一個集成的平台,用於對大規模基因數據進行系統性的分析,提供基因交互作用網路與路經分析,幫助科學家更深入了解基因如何偕同工作,參與分子生物學的機制。經由基因與交互作用間的探討,更可以讓科學家探索疾病的致病機轉,亦可以提供研究指引。IPA 利用視覺化的方式呈現結果,有助於研究者解譯研究的機轉成果。整體而言,IPA 對於研究人員在生物醫學研究和生物信息學分析中理解基因表達和生物學機制方面提供了有價值的支持。
簡介
結直腸癌(colorectal cancer, CRC) 為全球發病率第三高的癌症,在台灣,2019 年標準化發生率為每10萬人口42.9 人,發生人數已超過17,000 人,而死亡人數從109 年已增至6,489 人,標準化死亡率為每10 萬人口14.6 人,標準化死亡率上升9.8%。成為癌症發生率的首位,結直腸癌(Colorectal Cancer,CRC)是全球發病率第三高的癌症,也是全球癌症相關死亡的主要原因。
類似大多數癌症,結直腸癌轉移到遠端器官,如肝臟或肺部,是結直腸癌致命的主要原因。這種趨勢在大多數發達國家的老年人口中預計會加劇,因為老齡化是癌症的主要風險因素。儘管早期階段(I-II 期)僅侷限於結腸壁的CRC 在手術後應該是可以治愈的,但最終有高達25%的病例最終死於轉移。大約50%涉及淋巴結的III 期CRC 患者在手術後通常在5 年內死於轉移。IV 期CRC 是在診斷時就有遠端器官參與的轉移陽性病例。大多數CRC(80%)是零星發生的,通常發生在50 歲或以上的個體,其中環境因素如飲食和暴露於致癌物質以及遺傳易感性都可能導致疾病的發生。同樣,遺傳傾向可能在疾病的進展和轉移中發揮重要作用。然而,目前對於轉移的潛在生殖細胞基因因子仍然不明確。
研究方法
本研究由新加坡中央癌症醫院與新加坡國家癌症中心,自1996 收集至2018 年,零星型結直腸癌 (Sporadic colorectal cancer) 的病人,所有病例均根據臨床文件記錄的數據定義為轉移陽性或轉移陰性。患者的轉移陽性狀態是基於與原發性CRC 有關的遠端器官參與,至少5 年的隨訪期內未發現遠端器官的參與時,則確認為轉移陰性狀態。無法明確確認轉移狀態的病例被排除在分析之外。最後共採用1282 個轉移性結直腸癌與1397 個未轉移結直腸癌的病人。其採用 Affymetrix Genome-Wide Human SNP Array 6.0 定製 SNP 陣列進行全基因組關聯研究 (GWAS) 分析瞭解 SNP 陣列與結直腸癌是否會發生遠端轉移之關聯。
將變異位點資訊,利用FUMA 網站將變異位點及映射的基因集,包括整體和疾病亞型,進一步使用 Ingenuity Pathway Analysis(IPA)進行標準通路和比較分析。標準通路的識別使用Fisher 精確測試,並使用基於平均聯鎖和歐幾里得距離度量的分層聚合層次聚類算法進行分組。
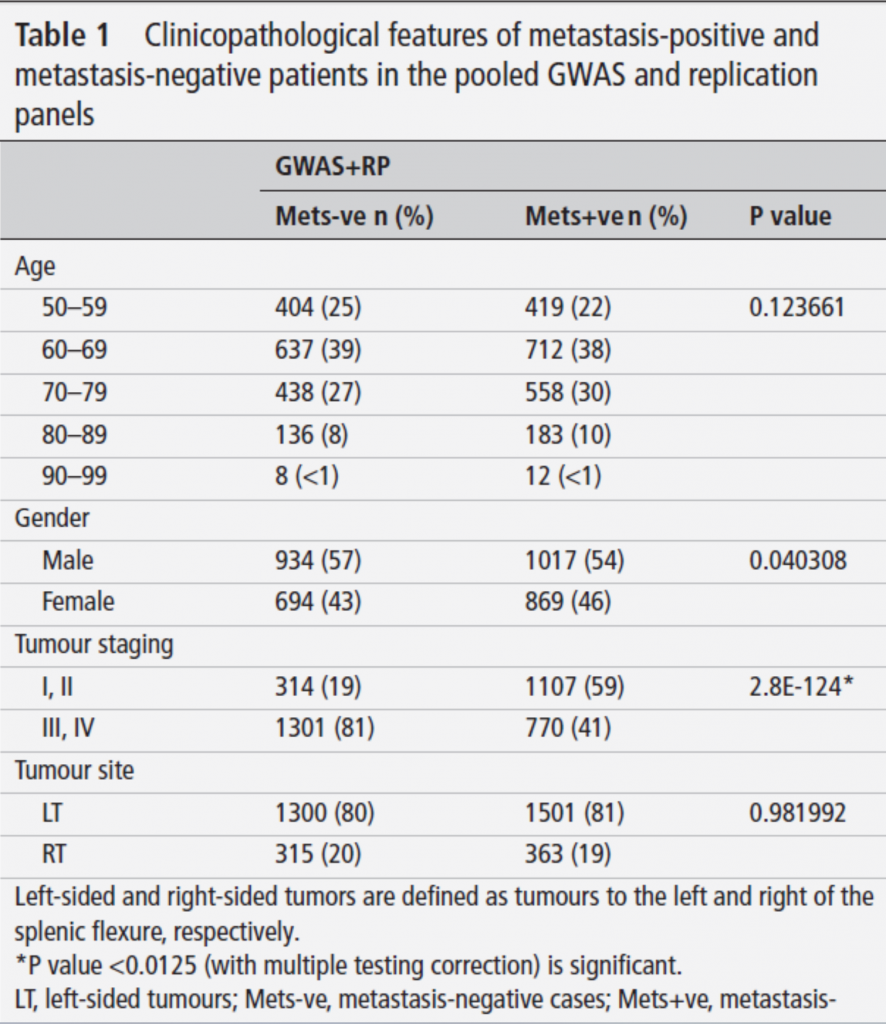
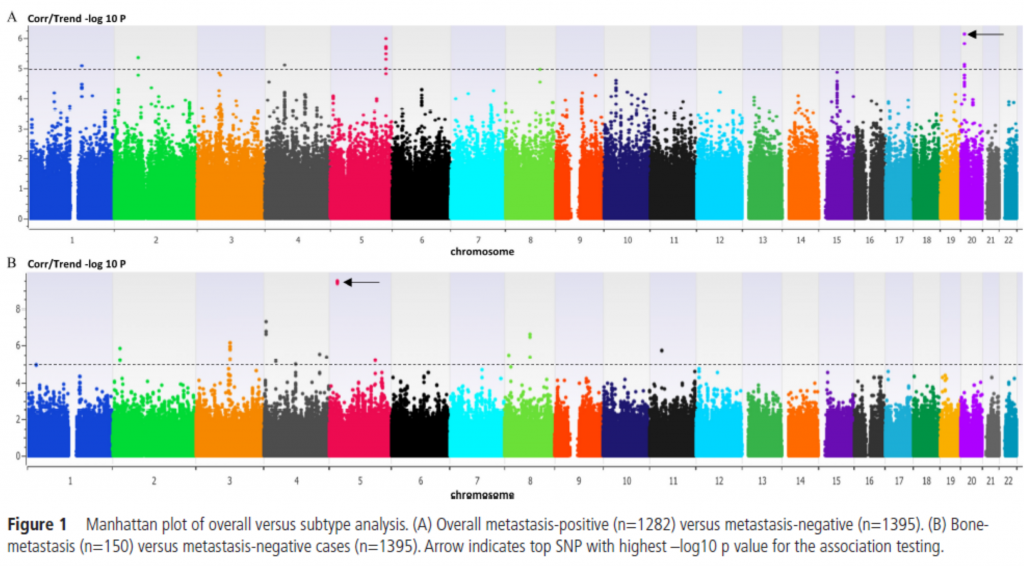
結果本篇研究使用1282 個轉移性結直腸癌與1397 個未轉移結直腸癌的病人,在轉移組與非轉移組的病患,年齡,腫瘤位置分布並無顯著差異,男性在轉移組中比例略高(p=0.04),作為轉移的代理終點的腫瘤分期在轉移陽性和轉移陰性病例之間有非常顯著的差異(P=2.8X 10⁻¹²⁴)(表 1)。在總體的 GWAS 的部分,有數個位置有 P 值小於 1x 10⁻⁵ 分別為 20p12, 4q12,以及 1q21,如 figure 1A,針對骨轉移與轉移陰性病患,為 rs16889360 如 figure 1b
IPA 分析
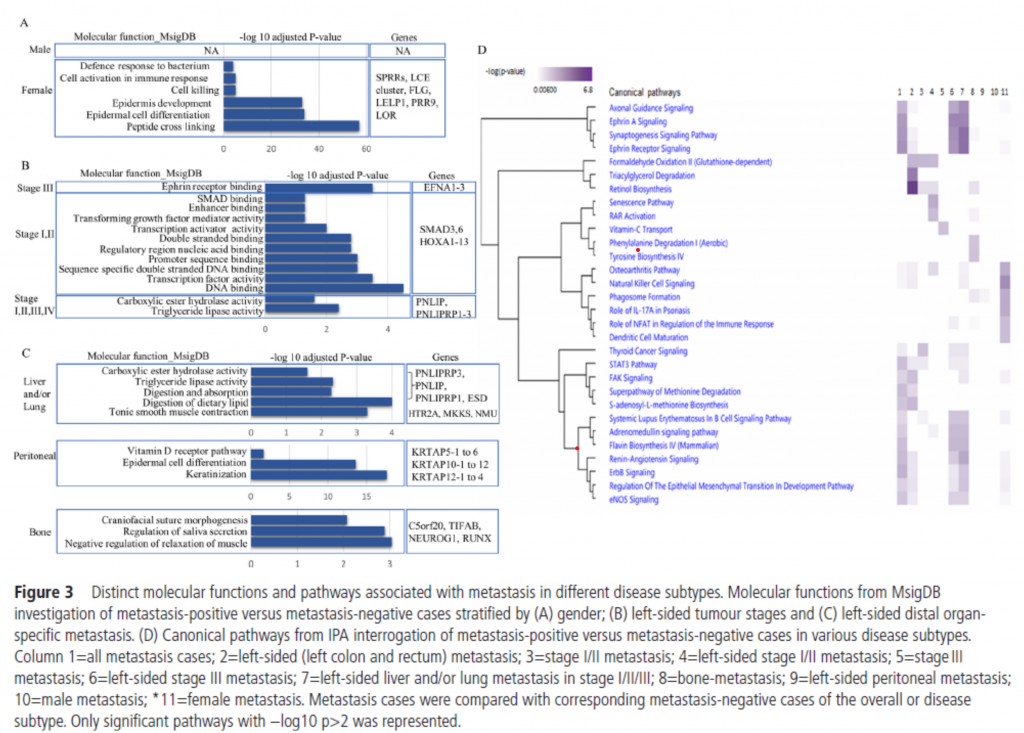
作者利用GWAS 找出與結直腸癌轉移相關的基因,並且導入IPA 進行後續的分析。分析結果顯示了30 個不同的標準通路,根據它們的相似性進行了分類(見圖3D)。這些通路涵蓋了從軸突導向信號到內皮一氧化氮合酶信號的各種通路。與所有病例最接近的具有顯著通路的疾病亞型是左側肝臟和/或肺部轉移在I/II/III 期,其次是左側III 期轉移。在省略右側結腸轉移病例的情況下,左側轉移在由谷胱甘肽依賴的甲醛氧化、三酰甘油降解和視網鉛生物合成通路組成的叢集中具有更高的顯著性。谷胱甘肽依賴的甲醛氧化通路在I/II 期轉移中也是顯著的,但在III 期轉移病例中缺失。左側I/II 期轉移還具有顯著的衰老和視網鉛酸受體(RAR)激活通路。骨轉移病例在包含苯丙氨酸降解和酪氨酸生物合成通路的叢集中具有顯著的標準通路,而這些通路在其他疾病亞型中找不到。值得注意的是,女性轉移病例(圖3D 的第11 列)具有一個獨特的顯著叢集,包括六個通路,從骨關節炎通路、自然殺傷細胞信號、吞噬體形成、白介素(IL-17)在牛皮癬中的激活,活化的T 細胞核因子調節到樹突細胞成熟,在男性轉移病例中這些通路並不顯著。
結論
這項研究的結果再次確認了CRC 是一種非常異質性的疾病,並且疾病亞型特定的轉移風險基因需要作為特徵納入到亞型特定的轉移易感受性的開發中,以進行臨床應用。IPA 協助作者深入研究CRC的亞型特定轉移風險。通過對不同疾病亞型的轉移陽性和轉移陰性病例進行標準通路分析,我們確認了30 個不同的標準通路,這些通路對不同的亞型具有獨特的關聯。這一結果不僅為我們對CRC轉移機制的理解提供了深入洞察,也為未來發展基於標準通路的亞型特定轉移簽名奠定了基礎。這項工作拓展了我們對CRC 異質性的理解,並為個體化的治療和管理提供了更精準的方向。
參考資料
https://pubmed.ncbi.nlm.nih.gov/37890997/